비칼루타미드
비칼루타미드 (比卡鲁胺)
Bicalutamide
경구 투여 (Oral)
비칼루타미드는 원래 전립선암 치료를 위해 개발된 강력한 비스테로이드성 안드로겐 수용체(AR) 길항제입니다. 트랜스젠더 HRT에서는 최후의 수단으로 사용하는 항안드로겐제로 — CPA, 스피로노락톤, GnRH 작용제 모두 사용 불가능한 경우에만 고려합니다. WPATH SOC 8은 일상적인 GAHT에 비칼루타미드를 명시적으로 권고하지 않습니다.
약리학적 특성
섹션 제목: “약리학적 특성”작용 기전
섹션 제목: “작용 기전”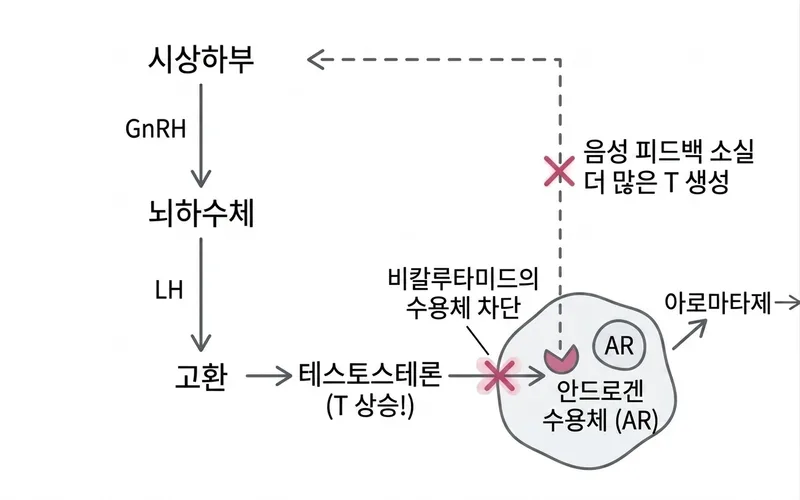
비칼루타미드는 현재 임상에서 가장 높은 친화도를 가진 비스테로이드성 AR 길항제 중 하나입니다:
- 강력한 AR 차단 (유일한 기전): 안드로겐 수용체에 경쟁적으로 결합하여 T와 DHT가 생물학적 효과를 발휘하지 못하도록 차단합니다
- 테스토스테론 수치 감소 없음: 피드백 기전으로 인해 T 수치가 오히려 상승할 수 있습니다
- GnRH-LH/FSH 축에 영향 없음: 시상하부-뇌하수체-성선 축을 억제하지 않습니다
약동학
섹션 제목: “약동학”- 경구 생체이용률: 약 90%
- 정상 상태 반감기: 5~6일 — 하루 복용을 놓쳐도 혈중 농도에 미치는 영향은 크지 않지만, 자주 놓쳐서는 안 됩니다
- 최고 혈중 농도 도달 시간: 약 31시간
- 정상 상태 도달 시간: 약 4주
T 수치 상승 문제
섹션 제목: “T 수치 상승 문제”이는 비칼루타미드를 GAHT에 사용할 때 나타나는 특수한 현상입니다 [1] :
- 비칼루타미드가 AR을 차단하면, 시상하부는 안드로겐 음성 피드백을 감지하지 못합니다
- 뇌하수체는 보상적으로 LH 분비를 증가시켜 고환이 더 많은 T를 합성하도록 자극합니다
- 혈청 T 수치는 투약 전의 1.5~2배까지 상승할 수 있습니다
- T의 생물학적 효과는 차단되지만, 높은 수치의 T는 방향화효소를 통해 에스트라디올로 전환될 수 있습니다
- 전립선암 환자에서 이러한 T 상승이 때때로 남성 유방 발달을 유발합니다
트랜스젠더 사용자에게 주는 시사점: AR이 차단되더라도, 높은 T 수치는 복약을 중단하거나 순응도가 낮아질 경우 남성화 효과가 빠르게 회복될 수 있음을 의미합니다.
용량 권고
섹션 제목: “용량 권고”| 방법 | 용량 | 설명 | 출처 |
|---|---|---|---|
| 시작/일반 | 25 mg/일 | 현재 대부분의 트랜스젠더 연구에서 사용되는 저용량 | Angus 2024; Burgener 2025 |
| 조정 범위 | 25~50 mg/일 | 임상 반응에 따라 조정 | Neyman 2019 (50mg); Angus 2024 (25mg) |
| 절대 상한선 | 50 mg/일 | 더 높은 용량은 추가 효과 없이 간독성 위험만 증가 | FDA 라벨 (전립선암 병용요법 용량) |
이상 반응
섹션 제목: “이상 반응”간독성 (가장 중요한 위험)
섹션 제목: “간독성 (가장 중요한 위험)”비칼루타미드의 간독성은 GAHT에서의 사용을 제한하는 주된 이유입니다 [1] :
FDA 라벨 데이터 (전립선암 임상시험 기반):
- 약 **6%**에서 일과성 무증상 ALT 상승 발생
- 약 **1%**에서 간염 또는 현저한 간 효소 상승으로 인해 투약 중단
- 150 mg 단독요법 대규모 시험(EPC, 8,113건): 비정상 LFT 3.4% (위약군 1.9%)
- 시판 후 최소 10건의 심각한 간 손상 증례 보고 발표, 그 중 2건 사망
트랜스젠더 인구 데이터 (근거는 제한적이나 참고할 만함):
- Neyman 2019: 청소년 23명, 50 mg/일, 임상적으로 유의한 간독성 없음 [2]
- Fuqua 2024: 청소년 40명 추적 관찰, 50 mg/일, 심각한 간 이상 없음 [3]
- Angus 2024: 성인 24명, 25 mg/일, 1명에서 경미한 간 효소 상승(가역적) [4]
- Wilde 2024: 증례 보고 1건, 50 mg/일, 간독성 발생(투약 중단 후 회복) [5]
이러한 데이터의 표본 크기는 여전히 너무 작아(총 약 170건), 드물지만 심각한 간 손상 위험을 배제할 수 없습니다.
폐독성 (간질성 폐질환)
섹션 제목: “폐독성 (간질성 폐질환)”FDA 라벨의 시판 후 경고에는 간질성 폐질환(ILD)이 포함되어 있으며, 간질성 폐렴 및 폐섬유증을 포함하고 일부 증례는 사망에 이르렀습니다.
- 전체 발생률 매우 낮음: 약 0.01%(1/10,000)로, 동종 약물인 닐루타미드(0.77%)보다 훨씬 낮습니다
- 일본 약물 감시 데이터: Matsumoto 2020은 일본 이상 반응 보고 데이터베이스(JADER)를 분석하여 비칼루타미드 ILD 보고 비율비가 9.2(95% CI 7.9~10.6)이며, 중간 발병 시간은 50일이라고 보고했습니다 [6]
유방 통증 및 발달
섹션 제목: “유방 통증 및 발달”- 비칼루타미드는 전립선암 환자에서 흔히 여성형 유방증(gynecomastia)을 유발합니다
- 트랜스젠더 사용자에서는 이 효과가 원하는 결과로 인식될 수 있습니다
- 유방 팽창통은 비교적 흔하게 발생합니다
기타 이상 반응
섹션 제목: “기타 이상 반응”- 홍조 (GnRH 작용제보다 덜 흔함)
- 위장관 불편감 (오심, 설사)
- 피부 건조
모니터링 요건
섹션 제목: “모니터링 요건”| 검사 항목 | 빈도 | 목표/경고 수치 | 처리 |
|---|---|---|---|
| 간 기능 (ALT/AST) | 기저치 + 첫 6개월간 매월 → 이후 3개월마다 | ALT/AST ≤ 정상 상한치 | > 3× 상한치: 즉시 투약 중단 후 의료 기관 방문 |
| 빌리루빈 | 간 기능 검사와 동시 | 정상 범위 | 상승 시 간 손상 악화 시사 |
| 테스토스테론 (T) | 3~6개월마다 | 참고용에 불과 (T 수치 상승 가능) | 효과의 주요 지표로 사용하지 않음 |
| 에스트라디올 (E2) | T와 동시 측정 | 100~200 pg/mL | 병용 방법 효과 평가 |
적용 시나리오
섹션 제목: “적용 시나리오”비칼루타미드는 GAHT에서 매우 제한적인 위치를 차지합니다 [1] :
다음 조건이 모두 충족될 때만 고려합니다:
- CPA를 사용할 수 없는 경우 (미판매/내약성 없음/수막종 위험)
- 스피로노락톤을 사용할 수 없는 경우 (신기능 저하/고칼륨혈증 위험/효과 불충분)
- GnRH 작용제를 사용할 수 없는 경우 (경제적/접근성 제한)
- 의사의 지도 및 정기적인 모니터링이 이루어지는 경우
금기사항:
- 기존 간질환 또는 간 기능 이상
- CPA 또는 기타 간독성 약물 복용 중
- 정기적인 간 기능 혈액 검사가 불가능한 경우
한국 내 접근 현황
섹션 제목: “한국 내 접근 현황”- 시판 상태: 비칼루타미드는 한국에서 시판 중 (전립선암 치료 적응증)
- 처방 경로: 비뇨기과 또는 종양내과에서 처방 가능
- 브랜드: 카소덱스(Casodex, 오리지널)와 국내 제네릭(예: 비카록, 비카루탄 등)
- 주의: 대부분의 의사들은 GAHT에서의 사용에 익숙하지 않으며, 처방을 받기 위해 전립선 관련 적응증을 언급해야 할 수도 있습니다
品牌图鉴
康士得 Casodex
- 厂商
- 阿斯利康 (AstraZeneca)
- 规格
- 50mg × 28片
- 外观
- 白色薄膜衣片
原研比卡鲁胺,价格较高
Calutide
- 厂商
- Cipla
- 规格
- 50mg
- 外观
- 白色薄膜衣片
Cipla 仿制比卡鲁胺,价格为原研的 1/5-1/10
Bicalox
- 厂商
- 多种印度厂商
- 规格
- 50mg
- 外观
- 白色薄膜衣片
印度仿制比卡鲁胺
Bicatero
- 厂商
- Hetero
- 规格
- 50mg
- 外观
- 白色薄膜衣片
Hetero 集团生产,全球仿制药大厂